Choque Cardiogênico
Avaliação e Manejo Baseado em Evidências
Apresentado por Laura Ricarte
Residente de Clinica Medica UFRR (R2)
Tipos de Choque: Perfil Hemodinâmico
| Tipo de Choque | PVC | POAP | DC/IC | RVS | SvO₂ | Fisiopatologia |
|---|---|---|---|---|---|---|
| Hipovolêmico | ↓ | ↓ | ↓ | ↑ | ↓ | Baixa pré-carga → baixo débito |
| Cardiogênico | ↑ | ↑↑ | ↓↓ | ↑ | ↓ | Falência de bomba → congestão |
| Distributivo (séptico) | ↓/N | ↓/N | ↑ | ↓↓ | ↑ | Vasoplegia + shunt |
| Distributivo tardio | ↓/N | ↓/N | ↓ | ↓ | ↓ | Depressão miocárdica séptica |
| Obstrutivo – TEP | ↑↑ | ↓/N | ↓ | ↑ | ↓ | Falência VD → baixo enchimento VE |
| Obstrutivo – Tamponamento | ↑↑ | ↑ | ↓ | ↑ | ↓ | Restrição diastólica global |
| Neurogênico | ↓ | ↓ | ↓ | ↓↓ | N/↑ | Perda de tônus simpático |
Cateter de Swan-Ganz
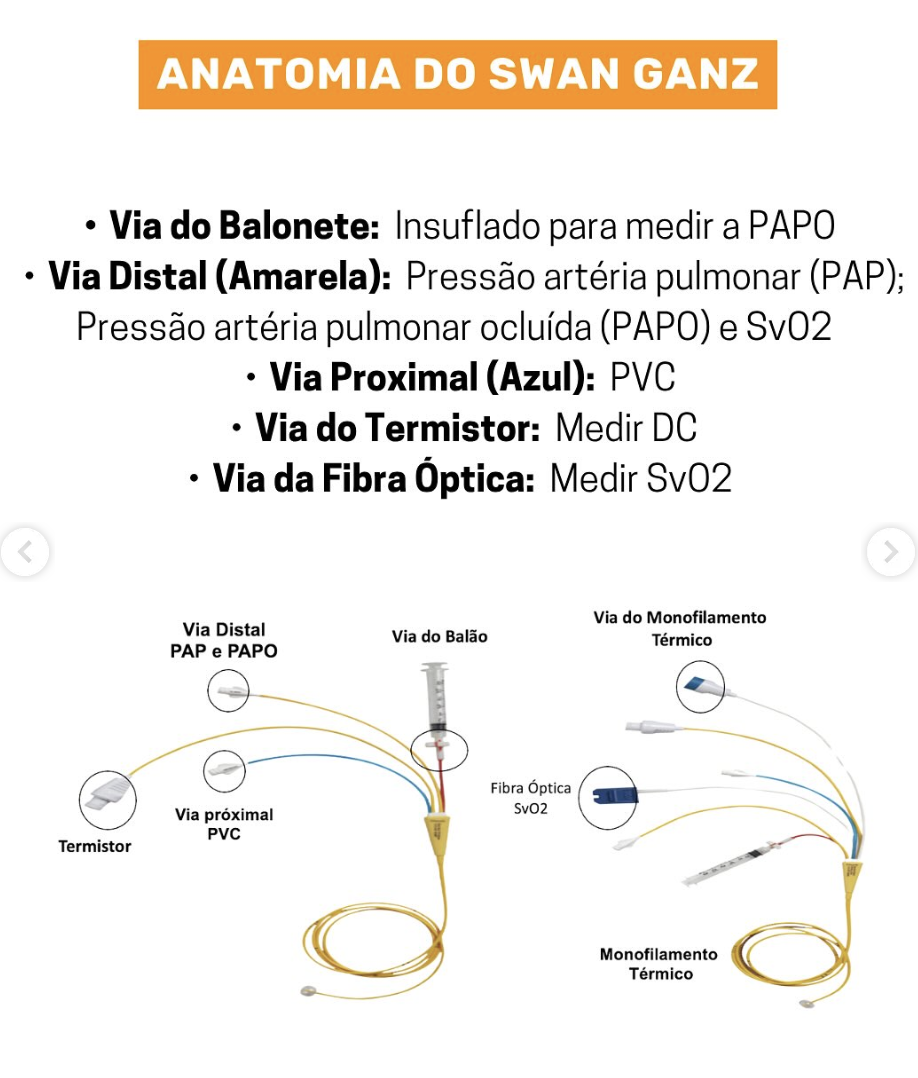
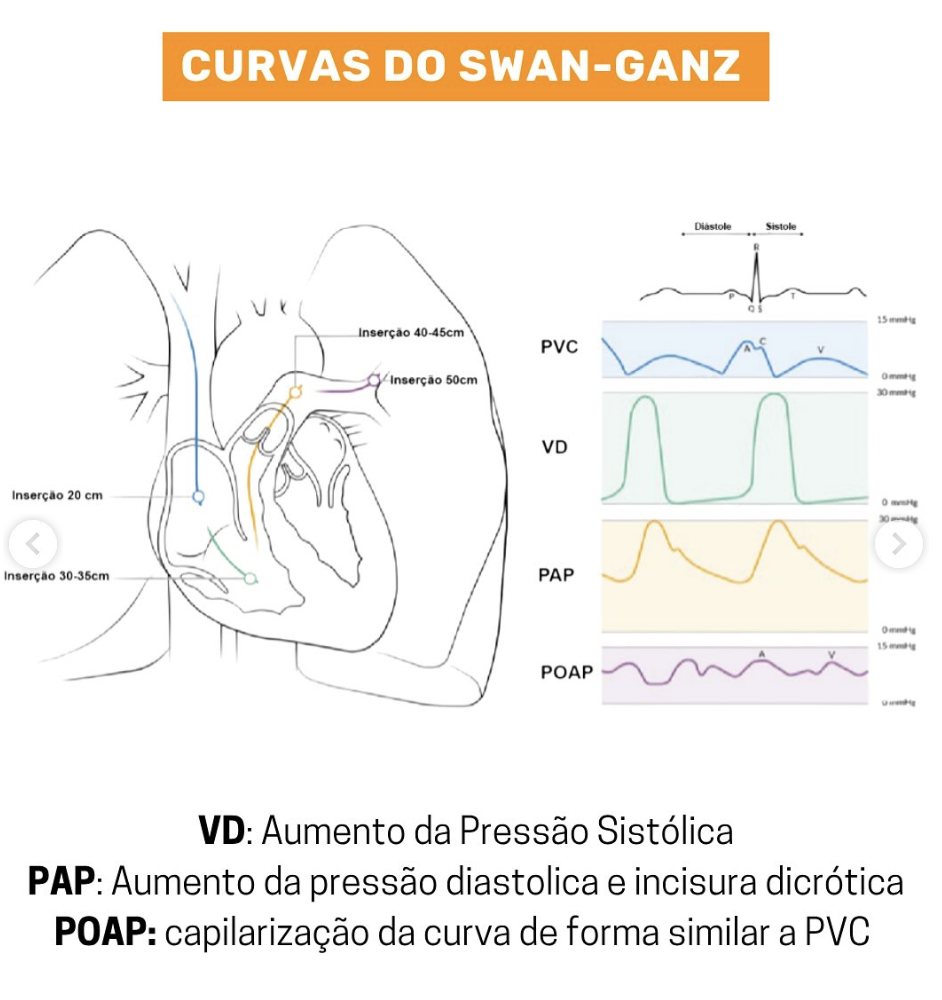

Monitorização hemodinâmica invasiva para avaliação do choque cardiogênico
Objetivos de Aprendizagem
Reconhecer Precocemente
Identificar sinais e sintomas do choque cardiogênico utilizando o mnemônico SUSPECT CS
Classificar a Gravidade
Aplicar a classificação SCAI (A-E) para estratificação de risco
Manejo Farmacológico
Compreender inotrópicos, vasopressores e suas indicações
Suporte Mecânico
Conhecer dispositivos de assistência circulatória temporária
O que e Choque Cardiogênico?
Distúrbio cardíaco que resulta em evidência clínica e bioquímica de hipoperfusão tecidual sustentada, independente da pressão arterial subjacente.
— SHARC (Shock Academic Research Consortium), 2023
Mortalidade em 30 dias
Mortalidade em 1 ano
Causa de morte no IAM hospitalizado
Critérios Diagnósticos
1 Hipotensão Sustentada
- PAS <90 mmHg por >30 min
- PAM <65 mmHg
- Queda >30 mmHg do basal
- Necessidade de DVA para manter PAS >90
2 Hipoperfusão Orgânica
- Lactato >2 mmol/L
- Oliguria (<0.5 mL/kg/h)
- Alteração do nível de consciência
- Extremidades frias e pegajosas
Atenção: Existe o Choque Cardiogênico Normotensivo — hipoperfusão organica com PAS >90 mmHg
Mnemônico SUSPECT CS
Ferramenta para diagnóstico precoce do choque cardiogênico
Etiologias do Choque Cardiogênico
AMI-CS (~50%)
Choque relacionado ao IAM
- • STEMI (~66%)
- • Non-STEMI (~30%)
- • Complicações mecânicas (~3%)
HF-CS (>50%)
Choque relacionado a IC
- • IC aguda "de novo" (~25%)
- • IC crônica agudizada (~75%)
- • Miocardite, Takotsubo, periparto
CS Secundario
Causa nãomiocárdica
- • Arritmias
- • Doença valvar aguda
- • Doença pericardica
Pos-cardiotomia
Após cirurgia cardíaca
- • Disfunção miocárdica pós-CEC
- • Stunning miocardico
Tendência atual: HF-CS está ultrapassando AMI-CS como causa mais frequente
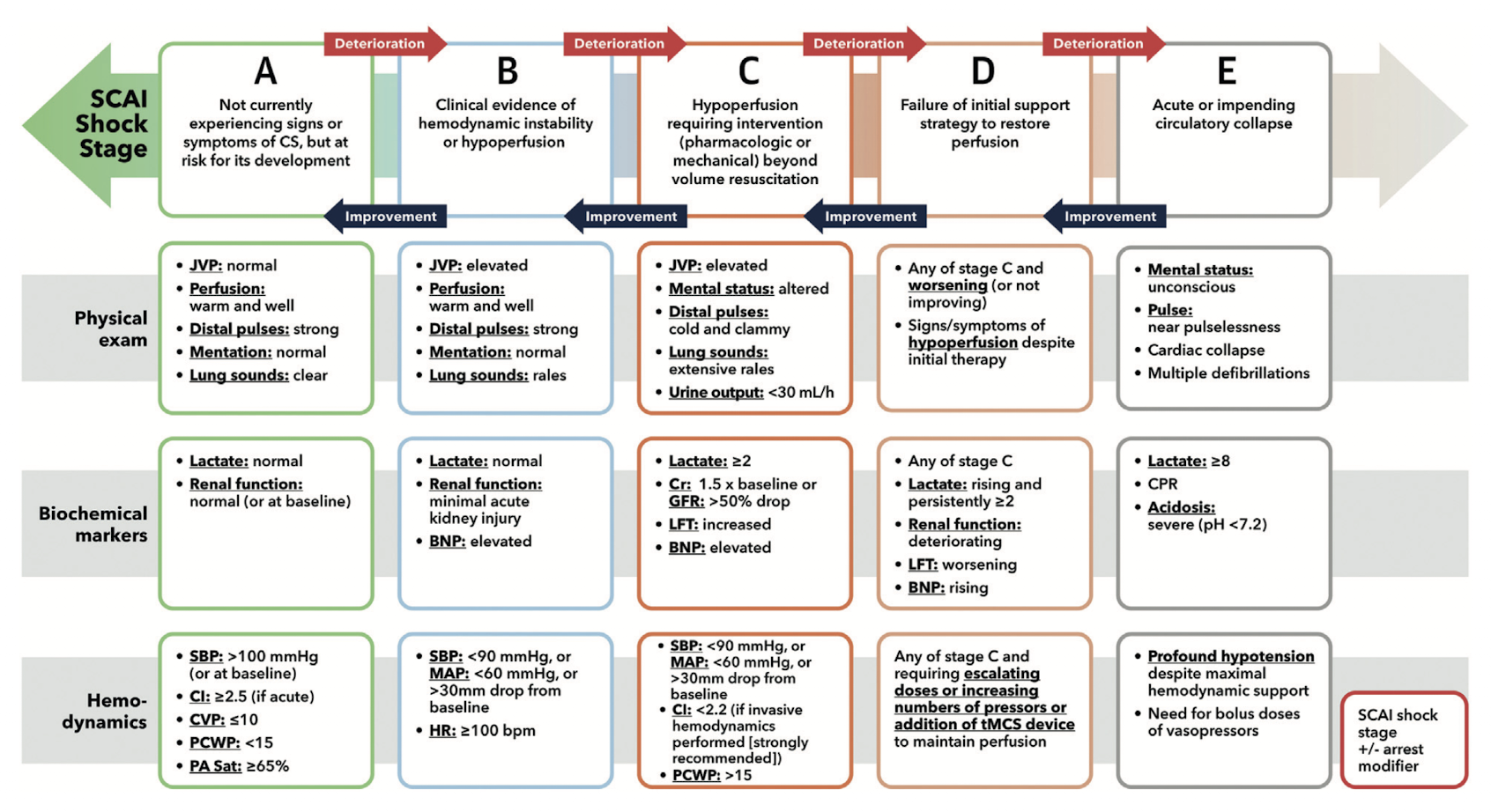
Classificação SCAI do Choque
At Risk
Risco de desenvolver choque
- • PAS normal
- • Lactato ≤2
- • Perfusão normal
- • IC >2.5
Ex: IAM extenso, IC avançada
Beginning
Pré-choque / Início
- • PAS <90 ou queda >30
- • FC ≥100 bpm
- • Lactato ≤2
- • Função renal normal
Maior risco de deterioração!
Classic
Choque clássico
- • Hipotensão + DVA
- • Lactato >2
- • IC <2.2
- • POAP >15
- • Hipoperfusão
Requer intervenção
Deteriorating
Deteriorando
- • Lactato ≥4 e subindo
- • Piora função renal
- • Piora função hepática
- • Escalando DVA
Falha na estratégia inicial
Extremis
Colapso circulatório
- • Lactato ≥8
- • pH <7.2
- • PCR ou iminente
- • Múltiplas DVAs
- • Colapso hemodinâmico
Suporte máximo
Fisiopatologia: Espiral Descendente
Função Cardiaca diminuída
Débito Cardíaco reduzido
Pressão Arterial reduzida
Hipoperfusão coronáriana
Perfusão Tecidual reduzida
Hipoxia celular - Lactato elevado
Vasoconstrição
Compensatoria inicial
Falência Multiorgânica
Rim - Fígado - Pulmão - Intestino - Coagulação
Fase Compensada
Vasoconstrição sistêmica mantem PA inicialmente
Fase Descompensada
Vasodilatação patológica por resposta inflamatória
Disfunção Multiorgânica no Choque
Baseado em NEJM 2026 - Thiele & Hassager
Cerebral
Hipoperfusão → Confusão
20-30% morrem por lesão anóxica pós-PCR
Pulmonar
Congestão, possível SDRA
↓ SpO₂
Hepática
Hepatite hipóxica
↑ AST, ALT, Bilirrubina
CORAÇÃO
↓ DC → Hipoperfusão sistêmica
↑ Troponina, ↑ BNP
Mortalidade 40-50% em 30 dias
Renal
IRA - Oligúria/Anúria
↑ Creatinina, ↑ Cistatina C
TRS: 11-18% nos trials
Intestinal
Translocação bacteriana
↑ Lactato, infecções
Microvascular
Vasoconstrição, microtrombos
Pele fria, TEC prolongado
Fenótipos e Prognóstico
Mortalidade Hospitalar por Etiologia
Berg et al. Eur Heart J Acute Cardiovasc Care 2024
Fenótipos Ventriculares
Falência VE dominante
Forma mais comum
Envolvimento VD
44% no CS-IAM; ainda mais comum em CS não-IAM
Biventricular
Pior prognóstico - requer estratégia específica
Importante: Fenótipo guia escolha de suporte mecânico e manejo de fluidos
PCR: ~50% dos CS-IAM têm PCR associada → alto risco de lesão cerebral anóxica
CS não-IAM: Agora supera CS-IAM em frequência → importância crescente
Roadmap das Primeiras 24 Horas
0-30 min
Avaliação Inicial
- • SUSPECT CS
- • ECG 12 derivações
- • Echo/POCUS
- • Labs: lactato, troponina
- • Classificação SCAI
30-90 min
Manejo Inicial
- • Shock team ativado
- • Iniciar DVA
- • Cate cardíaco +/- ICP
- • +/- Cateter de Swan-Ganz
- • +/- tMCS
6-12 horas
Estabilização
- • Reavaliação seriada
- • Monitorar trajetoria
- • Otimizar terapia
- • Alvos hemodinâmicos
- • Descongestão
12-24 horas
Definição de Estratégia
- • Escalonar/reconfigurar tMCS
- • Avaliar "exit strategy"
- • Recuperação vs LVAD vs Tx
- • Considerar cuidados paliativos
Monitorização Hemodinâmica
Cateter de Arteria Pulmonar
Indicações no Choque Cardiogênico:
- • Sem resposta a terapia inicial
- • Incerteza diagnóstica/terapêutica
- • Choque misto (cardiogênico + distributivo)
- • Guiar manejo de tMCS
Associado a menor mortalidade em estudos observacionais
Valores no Choque Cardiogênico
Potência cardíaca = melhor preditor de mortalidade no CS
CPO = (IC × PAM) / 451 · Normal ~1W
CPO (Cardiac Power Output) é o preditor hemodinâmico mais forte de mortalidade no CS
Manejo Farmacológico
Inotrópicos
Aumentam Contratilidade miocárdica
- • Dobutamina
- • Milrinona
- • Levosimendan*
Vasopressores
Aumentam Resistência vascular
- • Norepinefrina (1a linha)
- • Vasopressina
- • Fenilefrina (evitar)
Inopressores
Aumentam Contratilidade + RVS
- • Epinefrina
- • Dopamina (evitar)
Princípio fundamental: Usar na menor dose possível pelo menor tempo possível
Inotrópicos: Mecanismos de Ação
Inotrópicos aumentam a contratilidade miocárdica independente de pré-carga e pós-carga
Calcitropes
Efeito inotrópico verdadeiro
↑ Cálcio intracelular → maior força de contração
Cronotrópicos
Aumentam frequência cardíaca
DC = FC × VS (sem melhorar contratilidade)
Pode aumentar consumo de O₂ miocárdico
Inopressores
• ↑ Contratilidade + ↑ RVS
Indicação: Choque com hipotensão grave
Inodilatadores
• ↑ Contratilidade + ↓ pós-carga
Indicação: Baixo débito com PA preservada
Algoritmo: Terapia Vasoativa
Estratificação pelo fenótipo hemodinâmico guia a escolha terapêutica inicial
Hipotensão
PAS <90 ou PAM <65 mmHg
1ª Linha: NORADRENALINA
• Dose: 0,1 - 2 μg/kg/min
• Ação α1 predominante → ↑RVS
Refratário: + Vasopressina ou Epinefrina
Baixo Débito
PA ok + sinais de hipoperfusão
1ª Linha: INODILATADOR
• Dobutamina: 2-20 μg/kg/min
• Milrinona: 0,25-0,75 μg/kg/min
Milrinona se: β-bloqueador ou HP
SOAP II
Nora > Dopamina
(menos arritmias)
CAPS
Nora > Epinefrina
(menos refratário)
DOREMI
Milri = Dobuta
(CS pós-IAM)
Escolha do Agente: Guia Prático
Hipotensão grave
Alt: + Vasopressina
PA ok + Congestão
Alt: Milrinona
Uso de β-bloq
Não depende de β
Falência VD
↓RVP • Alt: +Nora
Bradicardia
Cronotrópico +
Misto/Vasodilat
↑PA + ↑DC
Usar com Cautela
- •Dopamina: mais arritmias vs Nora
- •Epinefrina: ↑lactato, ↑arritmias
- •Milrinona: meia-vida longa (cuidado IRA)
Metas Terapêuticas
- ✓ PAM ≥65 mmHg (individualizar)
- ✓ IC >2.2 L/min/m²
- ✓ Lactato em queda
- ✓ DU >0.5 mL/kg/h
Vasoativos: Doses e Preparo
Noradrenalina
Vasopressor de 1ª linha
Dose: 0,1-2 μg/kg/min
Preparo: 4mg/250mL SF (16 μg/mL)
Efeitos adversos: Isquemia periférica, arritmias
Dobutamina
Inodilatador β1-agonista
Dose: 2-20 μg/kg/min
Preparo: 250mg/250mL SF (1mg/mL)
Efeitos adversos: Hipotensão, taquicardia, arritmias
Milrinona
Inibidor PDE-3
Dose: 0,25-0,75 μg/kg/min
Preparo: 20mg/200mL SF (100 μg/mL)
Efeitos adversos: Hipotensão, arritmias; ajustar se IRA
Vasopressina
Agonista receptor V1
Dose: 0,01-0,04 U/min (fixa)
Preparo: 20U/100mL SF (0,2 U/mL)
Efeitos adversos: Isquemia mesentérica/digital
Dica: Evitar bolus de Milrinona no choque (risco de hipotensão grave). Preferir infusão contínua direta.
Agentes Vasoativos: Mecanismos
| Agente | Receptores | RVS | PA | DC | FC |
|---|---|---|---|---|---|
| Norepinefrina | a1+++, b1++ | ++ | ++ | + | + |
| Epinefrina | b1+++, a1++, b2++ | ++ | ++ | ++ | ++ |
| Dobutamina | b1+++, b2++ | -/0 | -/0 | ++ | + |
| Milrinona | Inibidor PDE-3 | -- | -- | ++ | 0/+ |
| Vasopressina | V1 receptor | ++ | ++ | 0/- | 0/- |
1a Linha: Norepinefrina
Pacientes hipotensos - melhor perfil de seguranca que dopamina
Alvo: PAM >65 mmHg
Estudo NorShock em andamento: PAM 55 vs 65 mmHg
Suporte Circulatório Mecânico (tMCS)
Objetivos
- 1. Descarregar o ventriculo (unloading)
- 2. Restaurar perfusão sistêmica
- 3. Permitir desmame de DVAs
Estratégias de Ponte
- • Bridge to Decision
- • Bridge to Recovery
- • Bridge to LVAD
- • Bridge to Transplant
Ponto-chave: Uso rotineiro de tMCS em TODOS os pacientes com CS não é recomendado. Seleção adequada do paciente é fundamental.
Dispositivos de tMCS
BIA
Balão Intra-aórtico
- • Fluxo: 0.5-1 L/min
- • Aumenta Perfusão coronária
- • Diminui pós-carga
- • Fácil inserção
IABP-SHOCK II: sem benefício mortalidade
Impella
Bomba microaxial
- • CP: 3-4.3 L/min
- • 5.5: 5-6 L/min
- • Descarrega VE diretamente
- • Aumenta Perfusão coronária
DanGer Shock: diminui mortalidade em STEMI selecionado
VA-ECMO
Oxigenação por membrana
- • Fluxo: 5-7 L/min
- • Suporte VE + VD + respiratório
- • Aumenta pós-carga (problema)
- • Pode necessitar unloading
ECLS-SHOCK: sem benefício mortalidade
pRVAD
Suporte VD percutaneo
- • Impella RP: 3-4 L/min
- • Protek Duo: 4-5 L/min
- • Para falência VD
- • Pode combinar com suporte VE
Estudos randomizados limitados
TandemHeart
AE → Artéria Femoral
- • Fluxo: até 4 L/min
- • Drena sangue do AE
- • Bypassa completamente o VE
- • Diminui pressões de enchimento
Evidência limitada; uso menos frequente
BIA vs Impella: Mecanismos de Ação
Balão Intra-Aórtico
Contrapulsação
Mecanismo
Balão na aorta descendente sincronizado com ECG
Infla na DIÁSTOLE
↑ Perfusão coronariana
↑ Perfusão sistêmica
Desinfla na SÍSTOLE
↓ Pós-carga (afterload)
↓ Trabalho do VE
IABP-SHOCK II (2012)
Sem benefício na mortalidade em 30 dias no IAM com CS
Ainda usado como ponte ou em combinação com outros dispositivos
Impella
Bomba Microaxial
Mecanismo
Bomba atravessa válvula aórtica: aspira sangue do VE e ejeta na aorta
Efeitos Hemodinâmicos
- • Descarrega diretamente o VE (↓ POAP, ↓ volume diastólico final)
- • ↑ Débito cardíaco efetivo
- • ↑ Perfusão coronariana (↑ PAM + ↓ pressão VE)
- • ↓ Consumo de O₂ miocárdico
Modelos e Fluxo:
CP
3-4.3 L/min
5.5
5-6 L/min
RP
VD: 4 L/min
DanGer Shock (2024)
↓ 12.7% mortalidade absoluta em STEMI selecionado
HR 0.74 (IC 95%: 0.55-0.99) - Primeiro RCT positivo!
BIA: Suporte indireto por contrapulsação · Impella: Suporte direto com unloading ativo do VE
VA-ECMO: Suporte Máximo e o Problema do VE
VA-ECMO
Oxigenação por Membrana Extracorpórea
Mecanismo
Drena sangue venoso (AD/veia femoral) → Oxigena externamente → Retorna ao sistema arterial (aorta/femoral)
Capacidades
- • Suporte circulatório completo (5-7 L/min)
- • Suporte respiratório (oxigenação + remoção CO₂)
- • Suporta falência biventricular
- • Independe de ritmo cardíaco
ECLS-SHOCK (2023)
Sem benefício na mortalidade em 30 dias
Mais complicações (sangramento, isquemia de membro)
O Problema: Distensão do VE
VA-ECMO retorna sangue na aorta → ↑ pós-carga
Consequências no VE doente:
- • VE não consegue ejetar contra a pós-carga aumentada
- • Distensão do VE → ↑ tensão de parede
- • ↑ Consumo de O₂ miocárdico
- • Estase sanguínea → risco de trombo intracavitário
- • Edema pulmonar pode piorar
Sinais de distensão do VE:
- • Ausência de pulsatilidade na linha arterial
- • ↑ POAP persistente
- • Edema pulmonar progressivo
- • Ecocardiograma: VE dilatado, válvula aórtica não abre
Estratégias de LV Venting (Descompressão)
Impella
"ECMELLA"
Mais efetivo
BIA
Contrapulsação
↓ pós-carga
Septostomia
Atrial
Shunt AE→AD
Vent cirúrgico
Direto no VE/AE
Invasivo
A necessidade de venting deve ser avaliada rotineiramente em pacientes em VA-ECMO
VD pRVAD - Suporte de Ventrículo Direito
Falência de VD ocorre em 30-40% dos pacientes com CS e é preditor independente de mortalidade
Impella RP
- • Fluxo: até 4 L/min
- • Acesso: veia femoral → AD → AP
- • Bomba microaxial (similar ao Impella CP)
- • Aprovado para falência VD pós-LVAD ou pós-cardiotomia
Protek Duo
- • Fluxo: 4-5 L/min
- • Acesso: veia jugular interna
- • Cânula duplo-lúmen (AD → AP)
- • Pode ser conectado a oxigenador (suporte respiratório)
Indicação: Falência VD isolada ou BiV (em combinação com suporte VE)
Algoritmos de Manejo: tMCS por Etiologia
Clique nas imagens para ampliar
AMI-CS Management
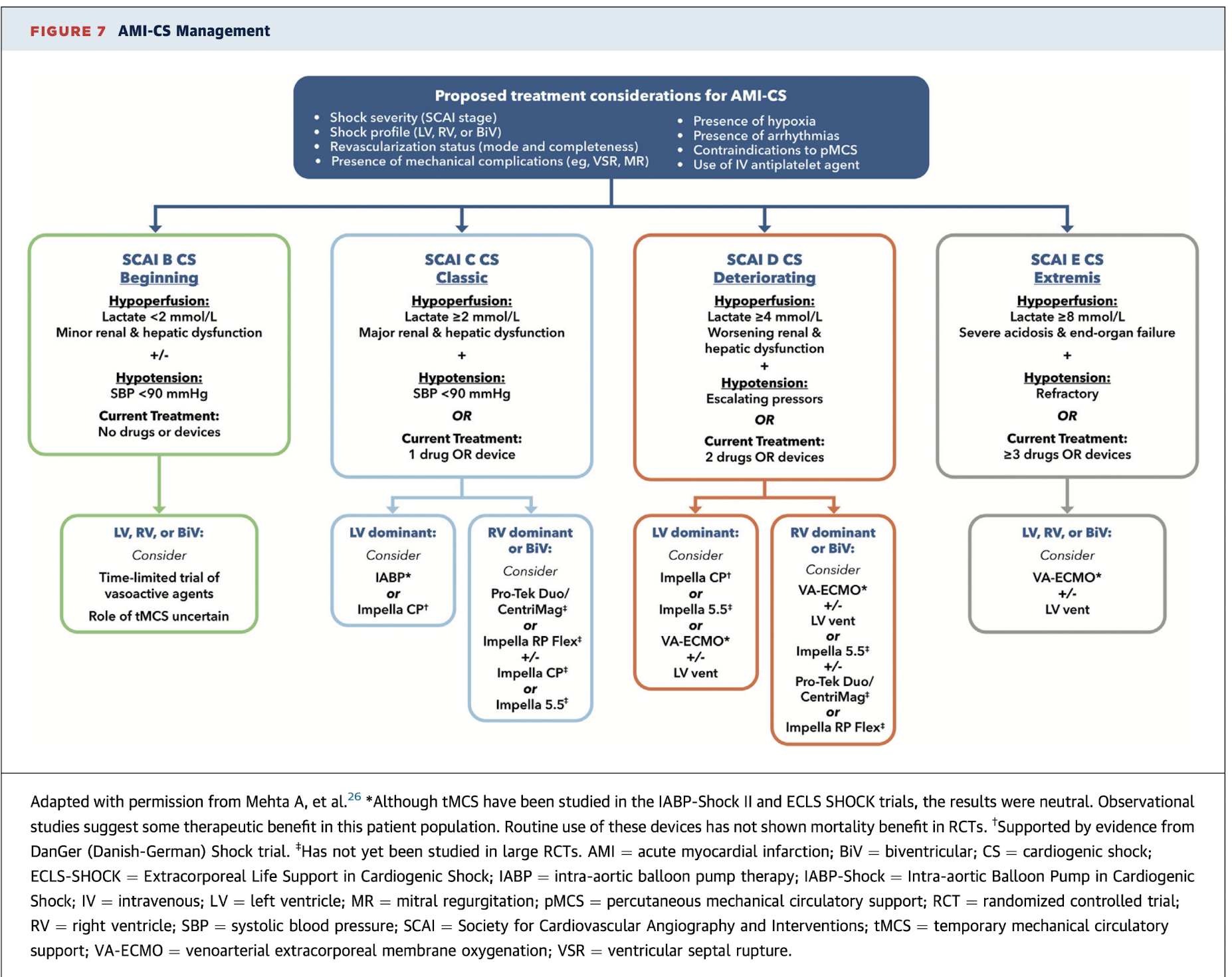
Adaptado de Mehta A, et al. - ACC 2025
HF-CS Management
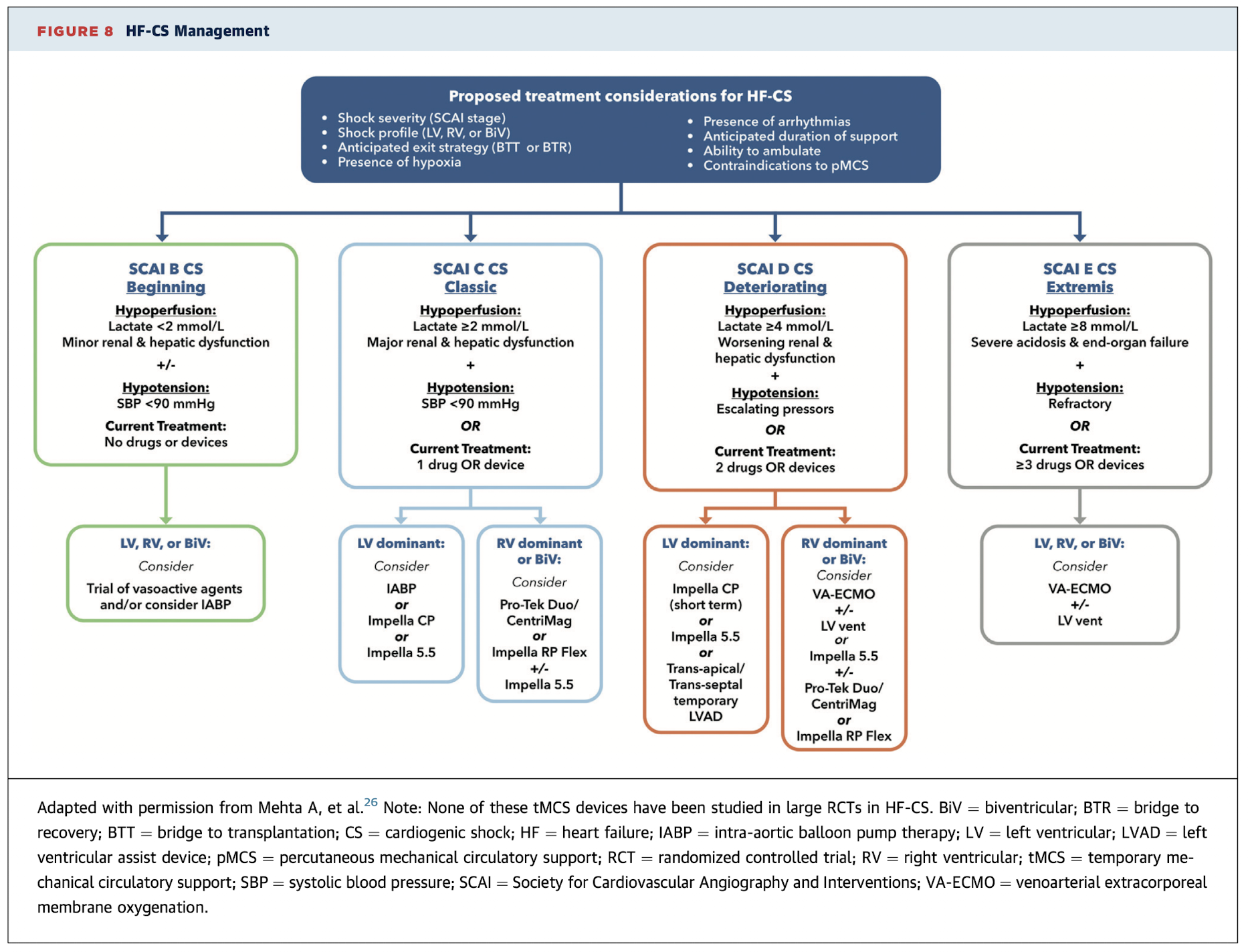
Adaptado de Mehta A, et al. - ACC 2025
Nota: Escolha do dispositivo depende de: estágio SCAI, fenótipo ventricular (VE/VD/BiV), estratégia de saída e disponibilidade local
DanGer Shock Trial (2024)
O primeiro RCT a demonstrar benefício de mortalidade com tMCS
Desenho do Estudo
- População: STEMI com CS, sem risco de lesão cerebral hipóxica
- n: 360 pacientes
- Intervenção: Impella CP precoce vs cuidado padrão
- Endpoint: Mortalidade em 180 dias
Resultados
-12.7%
Redução absoluta de mortalidade
HR 0.74
IC 95%: 0.55-0.99, p=0.04
Complicações aumentadas
Maior sangramento, isquemia de membro, necessidade de TRS
Seleção rigorosa
Apenas ~5-10% dos pacientes com CS preenchem criterios
Seleção de Pacientes para tMCS
Considerar tMCS
- • STEMI com CS VE-dominante (Impella - evidência DanGer)
- • Deterioração apesar de DVAs
- • Candidato a LVAD/transplante
- • Sem lesão cerebral hipóxica significativa
- • Centro com expertise em dispositivos
Não usar rotineiramente
- • Todos os pacientes com CS (sem benefício demonstrado)
- • Lesão cerebral anóxica estabelecida
- • Doença terminal / não candidato a terapias avançadas
- • Choque muito avançado com FMO irreversível
- • Doença vascular periférica grave (relativo)
50-60% dos pacientes com AMI-CS sobrevivem sem tMCS - Seleção inadequada pode causar complicações desnecessárias
Revascularização no AMI-CS
Revascularização precoce = Menor Mortalidade
Unica intervenção com evidência robusta de benefício de mortalidade no AMI-CS
SHOCK Trial: benefício sustentado ate 6 anos
Estratégia Recomendada
CULPRIT-SHOCK Trial
- • ICP culpado-only vs ICP multiarterial imediata
- • Culpado-only: 45.9% morte/TRS
- • Multiarterial: 55.4% morte/TRS
- • RR 0.83 (p=0.01)
Niveis de Centros de Choque
Nível 1
Centro Completo de CS
Nível 2
STEMI/ICP + opções de tMCS
Nível 3
Diagnóstico inicial (sem ICP/tMCS)
Nível 1
- • Hemodinâmica 24/7
- • tMCS avançado (todos)
- • Cirurgia cardíaca
- • LVAD e transplante
- • UTI cardíaca especializada
Nível 2
- • ICP 24/7
- • BIA e/ou Impella
- • UTI com monitorização
- • Cardiologia intervencionista
Nível 3
- • Diagnóstico inicial
- • Estabilização
- • Transferência para nível superior
Transferência e Desfechos
- • Maior mortalidade em pacientes transferidos (principalmente HF-CS)
- • Em redes regionalizadas: desfechos comparáveis entre níveis
Preditores de Pior Prognóstico
HF-CS
- • Idade avançada
- • VM / TRS
- • Múltiplas DVAs
AMI-CS
- • IMC >28
- • Lactato >3
- • Piora função renal
CAP (HF-CS) e tMCS (AMI-CS) associados a melhores desfechos
Shock Team: Abordagem Multidisciplinar
TEAM
Benefícios Demonstrados
- • Maior uso de cateter de AP
- • Maior uso de tMCS avançado
- • Menor mortalidade ajustada por risco
- • Melhor comunicação e coordenação
Componentes Essenciais
- • Sistema de ativação rápida 24/7
- • Comunicação virtual e a beira-leito
- • Protocolos padronizados
- • Revisão de casos e melhoria contínua
Características do Choque
- • Classificação SHARC
- • Classificação SCAI
- • Perfil congestivo
- • Clearance de lactato
- • Disfunção multiorgânica
- • Fenotipagem
Seleção do Paciente
- • Instabilidade elétrica ou hemodinâmica
- • Gravidade da disfunção ventricular
- • Anatomia coronária complexa
- • Ponte para recuperação
- • Terapias avançadas
- • Objetivos de cuidado
Considerações Terapêuticas
- Farmacoterapia •
- Suporte circulatório mecânico •
- Expertise do operador •
- Melhores práticas de acesso vascular •
- Prognóstico neurológico se PCR •
- Contraindicações •
- • Equipes multidisciplinares de choque
- • Redes regionalizadas de choque
- • Equipe dedicada 24/7 na UTI cardíaca
- • Capacidade de LVAD e transplante
- • Consultoria subespecializada
Sistemas de Cuidado
Desmame de tMCS
Pré-requisitos
- • Causa subjacente tratada/melhorada
- • Estabilidade hemodinâmica
- • DVAs em doses baixas/estaveis
- • Função de órgãos melhorando
Processo
- • Redução gradual de fluxo
- • 0.5-1 L/min a cada 2-4 horas
- • Monitorar clínica + lactato
- • Ecocardiograma seriado
Exit Strategy
- • Recuperação miocárdica
- • LVAD durável
- • Transplante cardíaco
- • Cuidados paliativos
Framework ROSE
Recognize / Rescue
0-6 horas
- • Reconhecimento precoce
- • Ativar shock team
- • Iniciar DVAs
- • Considerar tMCS
Optimize
6-24 horas
- • Otimizar hemodinâmica
- • Definir fenótipo VE/VD
- • Ajustar suporte
- • Swan-Ganz se necessário
Stabilize
24-72 horas
- • Estabilização clínica
- • Suporte multiorgânico
- • Reavaliação contínua
- • Prevenir complicações
Exit / De-escalate
>72 horas
- • Desmame de tMCS/DVAs
- • Definir exit strategy
- • Recuperação/LVAD/Tx
- • Considerar paliação
Adaptado de ACC Expert Consensus 2025 - Manejo estruturado por fases
Complicações e Falência Multiorgânica
Neurológico
- • Delirium
- • AVC (embolico/hemorragico)
- • Lesão cerebral anóxica
Pulmonar
- • Congestão/edema
- • Lesão por VM
- • Pneumonia
Hematológico
- • Sangramento (ate 60%)
- • Coagulopatia
- • Hemolise (tMCS)
Renal
- • IRA (hipoperfusão)
- • Necrose tubular
- • TRS em 10-18%
Hepático
- • Hepatite hipóxica
- • Insuficiência hepática
- • Necrose hepatocelular
Vascular
- • Isquemia de membro (4x maior com tMCS)
- • Dissecção
- • Pseudoaneurisma
Cuidados Paliativos no CS
Consulta precoce de cuidados paliativos deve ser considerada simultaneamente ao início de tMCS
Quando Considerar
- • Choque refratário a múltiplas intervenções
- • Não candidato a LVAD/transplante
- • Lesão cerebral anóxica significativa
- • Comorbidades limitantes de prognóstico
- • Desejo do paciente/família
Papel da Equipe
- • Comunicação clara com família
- • Discussão de objetivos de cuidado
- • Tomada de decisão compartilhada
- • Conforto e dignidade no fim de vida
- • Suporte a família enlutada
Pontos-Chave
Mortalidade permanece 40-50% apesar dos avancos
Revascularização precoce da lesão culpada reduz mortalidade no AMI-CS
Impella mostrou benefício em pacientes selecionados com STEMI-CS (DanGer Shock)
BIA e VA-ECMO nãodemonstraram benefício de mortalidade rotineiramente
Seleção do paciente é fundamental - nem todo CS precisa de tMCS
Abordagem multidisciplinar com shock team melhora desfechos
Estudos em Andamento
PACCS
Cateter de AP vs sem cateter no HF-CS
ANCHOR
VA-ECMO + BIA vs tratamento padrão
UNLOAD-ECMO
VA-ECMO + Impella vs VA-ECMO isolada
NorShock
PAM alvo 55 vs 65 mmHg
LevoHeartShock
Levosimendan vs placebo
CAPITAL DOREMI-2
Dobutamina ou milrinona vs placebo
Muitas questões permanecem abertas - necessidade de mais pesquisa randomizada
Obrigada!
Duvidas?
Referências Principais
1. Sinha SS et al. 2025 Concise Clinical Guidance: ACC Expert Consensus Statement on Cardiogenic Shock. JACC 2025;85:1618-1641
2. Thiele H, Hassager C. Cardiogenic Shock. N Engl J Med 2026;394:62-77
3. Moller JE et al. Microaxial Flow Pump in Infarct-Related Cardiogenic Shock (DanGer Shock). N Engl J Med 2024;390:1382-1393
4. Naidu SS et al. SCAI SHOCK Stage Classification Expert Consensus Update. JACC 2022;79:933-946
Tipos de Choque: Perfil Hemodinâmico
| Tipo | PVC | POAP | DC/IC | RVS | SvO₂ |
|---|---|---|---|---|---|
| Hipovolêmico | ↓ | ↓ | ↓ | ↑ | ↓ |
| Cardiogênico | ↑ | ↑↑ | ↓↓ | ↑ | ↓ |
| Distributivo | ↓/N | ↓/N | ↑ | ↓↓ | ↑ |
| Obstrutivo – TEP | ↑↑ | ↓/N | ↓ | ↑ | ↓ |
| Obstrutivo – Tamponamento | ↑↑ | ↑ | ↓ | ↑ | ↓ |
| Neurogênico | ↓ | ↓ | ↓ | ↓↓ | N/↑ |
Perfil Hemodinâmico por Câmara
| Tipo | PVC | POAP | PAPi | Fisiologia |
|---|---|---|---|---|
| Falência VE | N / ↑ leve | ↑↑ | normal | Congestão pulmonar + baixo débito |
| Falência VD | ↑↑ | N / ↓ | ↓↓ | VD não ejeta → congestão sistêmica |
| Biventricular | ↑↑ | ↑↑ | ↓ | Falência global |
PAPi = Índice de Pulsatilidade da Artéria Pulmonar
Valores Hemodinâmicos Normais
| Parâmetro | Valor Normal |
|---|---|
| PVC | 2–6 mmHg |
| POAP | 6–12 mmHg |
| IC | 2,5–4 L/min/m² |
| RVS | 800–1200 dyn·s·cm⁻⁵ |
| SvO₂ | 65–75% |
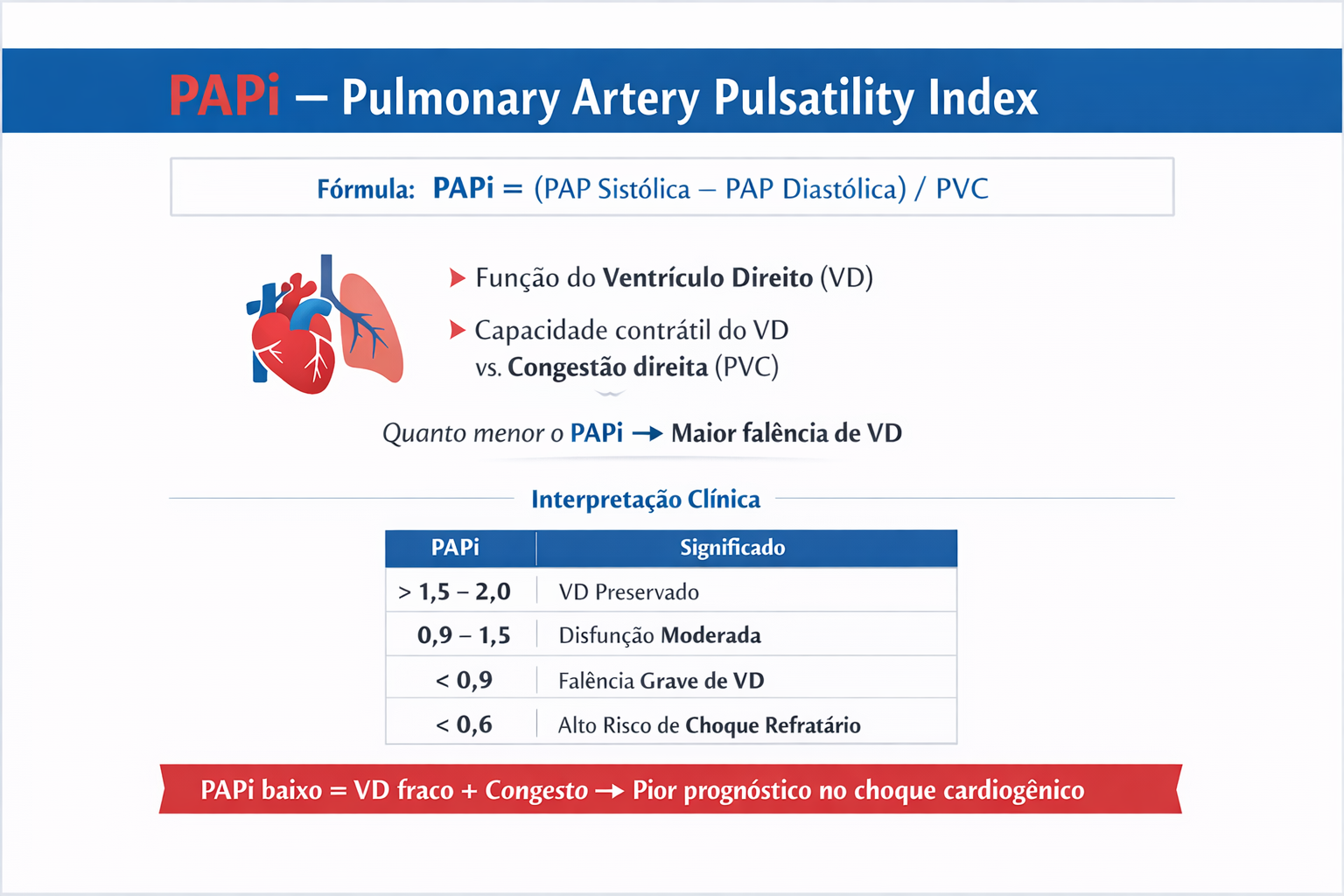
Comparação dos Dispositivos de Suporte Circulatório
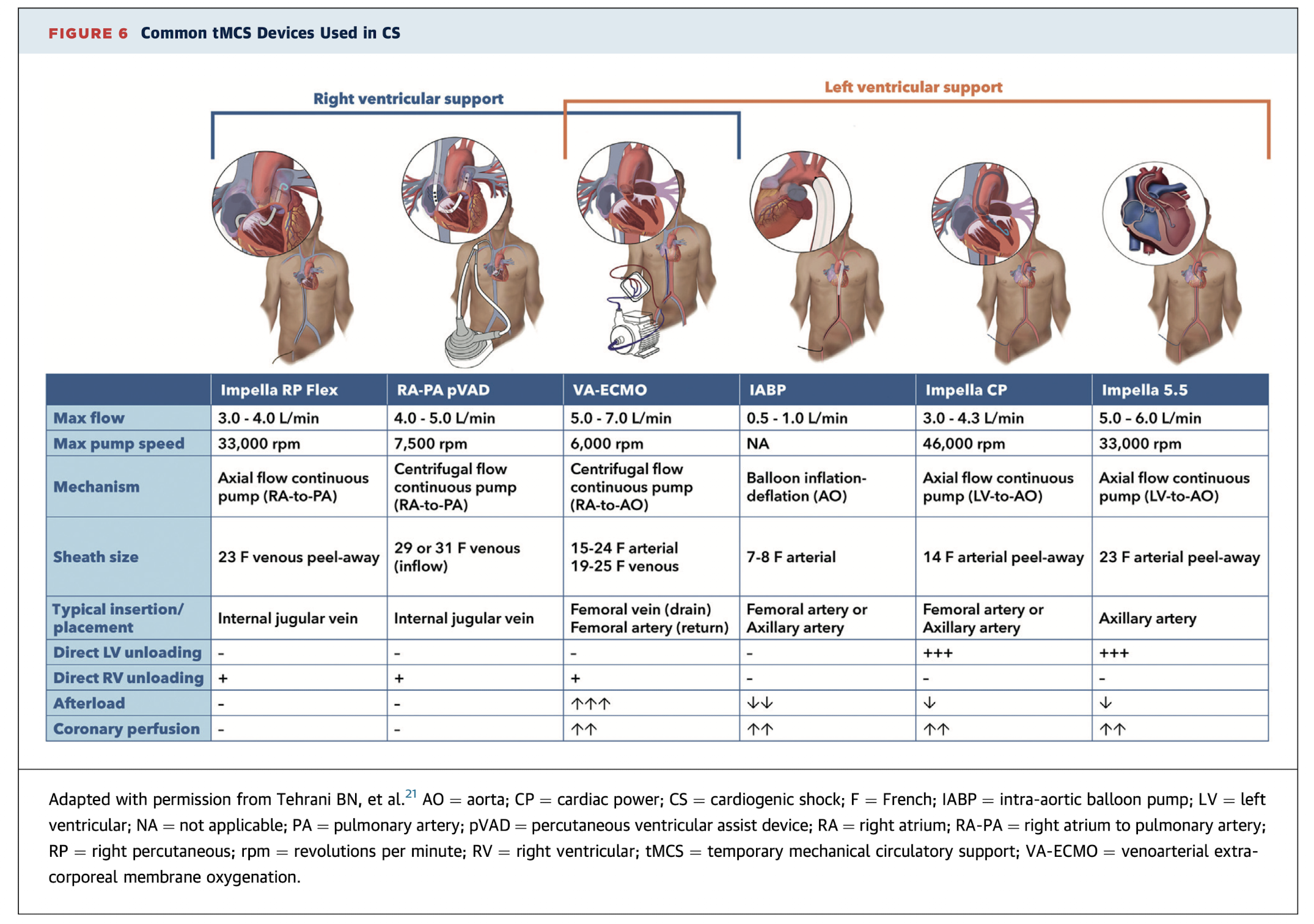
Use scroll do mouse para zoom · Arraste para mover a imagem
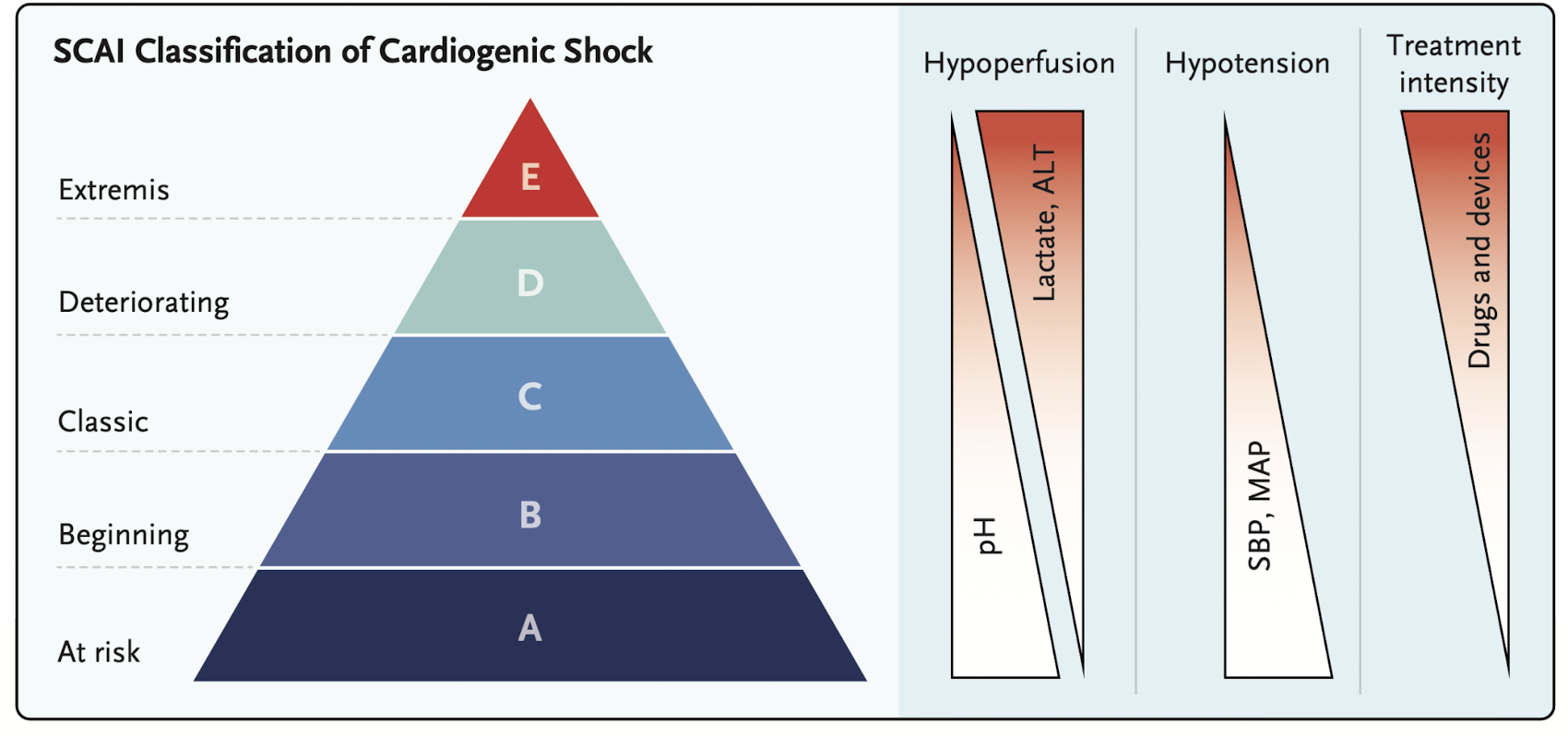
Receptores e Mecanismos de Ação
| Receptor | Localização | Efeito | Drogas |
|---|---|---|---|
| α1 | Vasos (músculo liso) | Vasoconstrição → ↑ RVS | Noradrenalina, Adrenalina, Fenilefrina |
| β1 | Coração (miócitos) | ↑ FC (cronotropismo) ↑ Contratilidade (inotropismo) | Dobutamina, Adrenalina, Isoproterenol |
| β2 | Vasos, brônquios | Vasodilatação → ↓ RVS Broncodilatação | Adrenalina, Isoproterenol, Dobutamina |
| PDE-3 | Coração e vasos | Inibe PDE-3 → ↑ AMPc Inotropismo + Vasodilatação | Milrinona |
| V1 | Vasos (músculo liso) | Vasoconstrição intensa (independente de catecolaminas) | Vasopressina |
PDE-3 = Fosfodiesterase 3 · AMPc = AMP cíclico · RVS = Resistência Vascular Sistêmica
HeartMate 3 LVAD
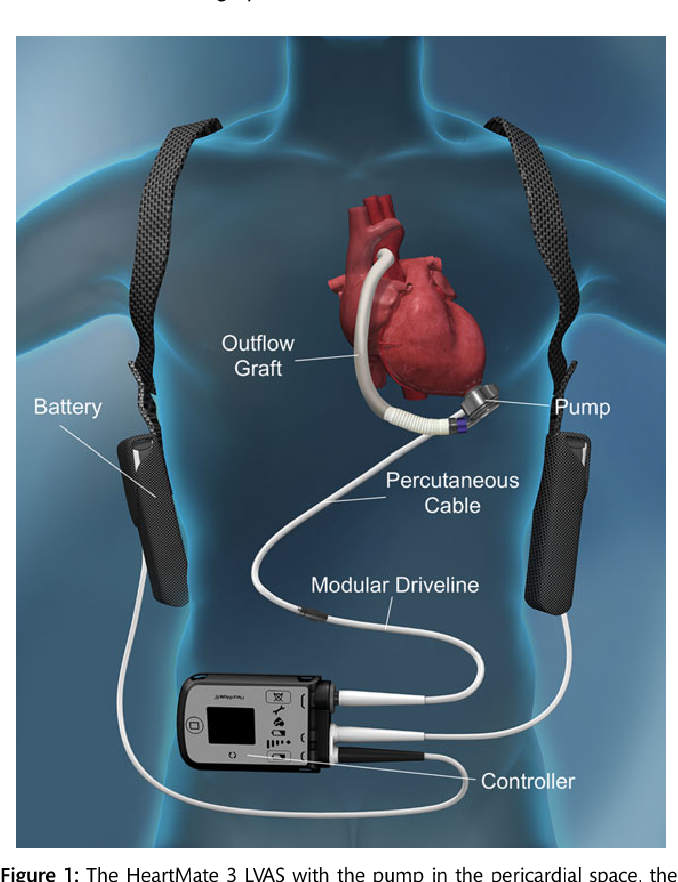
HeartMate 3 LVAD com bomba no espaço pericárdico, driveline modulável e controlador externo
AMI-CS Management

Adaptado de Mehta A, et al. - ACC Expert Consensus 2025
HF-CS Management

Adaptado de Mehta A, et al. - ACC Expert Consensus 2025
Reavaliação Estruturada na UTI
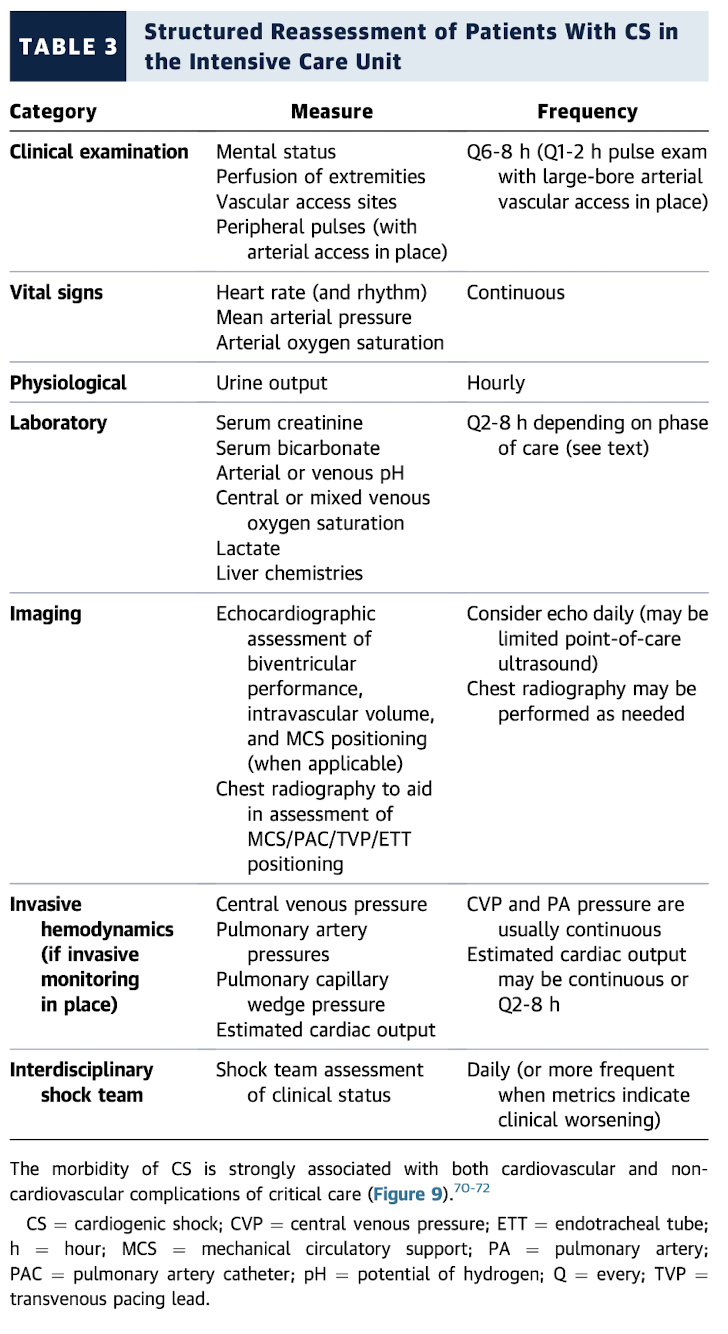
ACC Expert Consensus 2025 - Table 3
Balão Intra-Aórtico (BIA)
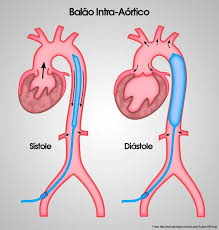
Contrapulsação: infla na diástole, desinfla na sístole
Impella
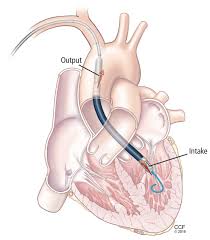
Bomba microaxial: aspira do VE (intake) e ejeta na aorta (output)